De l’espace pour bouger : le comportement des protéines en milieu encombré
12 Mai 2026La diffusion de neutrons révèle comment la densité locale influence le mouvement au sein des structures protéiques auto-assemblées.
-
Health

Au cœur des cellules vivantes, les protéines sont en mouvement constant, elles interagissent et s'organisent en structures complexes. Dans de nombreux cas, elles se regroupent en assemblages denses où l'espace est limité et le mouvement contraint. Comprendre le comportement des protéines dans ces environnements encombrés est essentiel pour expliquer des mécanismes biologiques fondamentaux, qu'il s'agisse de l'organisation cellulaire ou de la formation d'agrégats protéiques liés à certaines pathologies.
En utilisant la diffusion de neutrons à l’Institut Laue-Langevin, combinée à des simulations numériques, des chercheurs ont étudié le comportement d’un type spécifique de protéine au sein d’assemblages denses formés par les protéines elles-mêmes. Ils ont découvert que leur mouvement n'est pas uniforme : les protéines se déplacent plus lentement au cœur de ces assemblages et plus librement à leur périphérie. Cette observation démontre que l’auto-organisation des protéines influence directement leur mobilité, un effet crucial pour comprendre le fonctionnement des systèmes biologiques.

Un environnement encombré par auto-assemblage
Les protéines sont des molécules essentielles aux systèmes vivants. Elles se déplacent, interagissent et s'organisent pour assurer une multitude de fonctions, de la communication cellulaire à la formation de structures internes. Dans de nombreux cas, les protéines ne restent pas isolées : elles se regroupent spontanément pour former des assemblages composés de nombreuses molécules individuelles. Ce processus, appelé auto-assemblage, est piloté par les interactions entre les protéines elles-mêmes.
Ces assemblages créent des environnements très différents des liquides simples. Au lieu de se déplacer librement, les protéines sont entourées de nombreux voisins et l'espace peut devenir limité. Ces conditions d'encombrement sont très fréquentes à l'intérieur des cellules et peuvent fortement influencer la manière dont les molécules se déplacent et interagissent. Comprendre le comportement des protéines dans ces environnements est donc essentiel pour décrire le fonctionnement des systèmes biologiques.
Dans cette étude, des chercheurs ont examiné le comportement d'une protéine flexible, la β-caséine, au sein de tels assemblages. Pour ce faire, ils ont utilisé la diffusion de neutrons à l'Institut Laue-Langevin (ILL), combinée à des simulations numériques. Comme ces assemblages sont formés par les protéines elles-mêmes, ils créent un environnement « auto-encombré » où les conditions locales varient d'une région à l'autre. La β-caséine est un exemple de protéine intrinsèquement désordonnée, ce qui signifie qu'elle ne possède pas de structure stable et reste extrêmement flexible.
Les neutrons révèlent des mouvements complexes à l’échelle nanométrique
Pour observer directement ces effets, l’équipe a utilisé la diffusion quasi-élastique de neutrons (QENS) sur le spectromètre IN16B de l’ILL. Cette technique mesure d’infimes variations d'énergie des neutrons lors de leur interaction avec les atomes en mouvement dans l’échantillon étudié. Elle permet aux chercheurs de suivre le déplacement des molécules sur des échelles de temps extrêmement courtes (de la picoseconde à la nanoseconde, soit de quelques millièmes de milliardièmes à quelques milliardièmes de seconde) et sur de très petites distances (le nanomètre, soit un million de fois plus petit qu'un millimètre).
Les neutrons sont particulièrement adaptés à l’étude des protéines car ils sont très sensibles aux atomes d’hydrogène, abondants dans ces molécules. Cela permet de sonder le mouvement de chaînes protéiques individuelles même au sein d’assemblages denses, là où d’autres techniques peinent à accéder à de telles informations.
Dans un modèle simple, dit de diffusion fickienne, les molécules se déplacent de manière aléatoire mais globalement prévisible : bien qu'elles tendent à se propager des zones de forte concentration vers les zones de faible concentration, leur mouvement peut être décrit par une règle unique et uniforme à l'échelle du système.
Dans les assemblages de protéines désordonnées étudiés dans le cadre de cette étude, les mesures neutroniques révèlent un scénario différent. Au lieu d’un mouvement unique et uniforme, les données montrent un écart par rapport à la diffusion fickienne pour suivre un comportement connu sous le nom de diffusion de Singwi-Sjölander. Cela indique que le mouvement des protéines dépend de leur environnement immédiat au sein d’un même assemblage. Ce comportement se traduit directement dans le signal neutronique, qui ne peut alors plus être décrit par un processus de diffusion unique et simplifié.
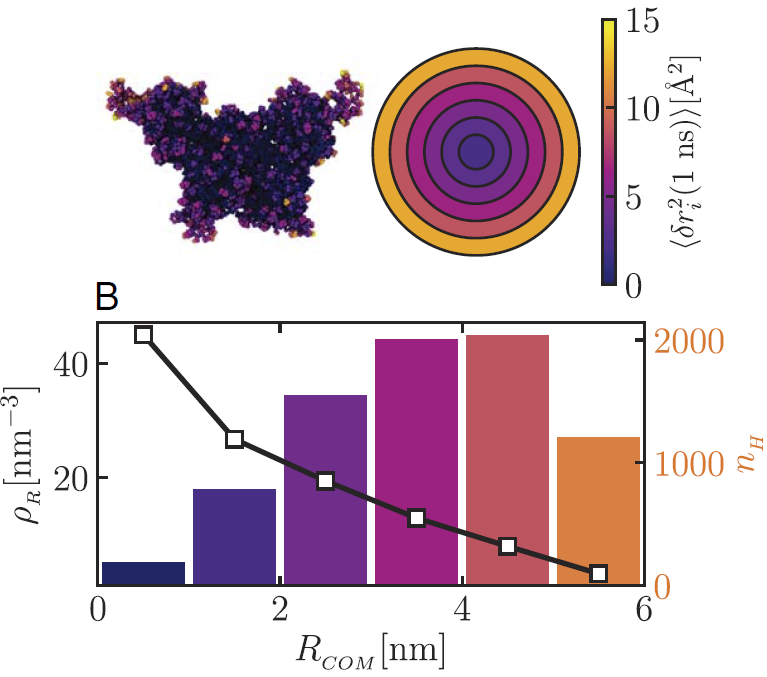
Le mouvement au sein d'un assemblage de protéines n'est pas uniforme. (En haut à gauche). L'assemblage est coloré selon l'amplitude du mouvement des protéines : le déplacement est plus lent dans le cœur dense (couleurs sombres) et plus rapide vers la périphérie (jaune). (En haut à droite) Vue simplifiée montrant la transition graduelle de ce mouvement du centre vers l'extérieur. (En bas) Distribution du matériel protéique en fonction de la distance par rapport au centre de l'assemblage (RCOM). La ligne noire représente la densité de compactage des protéines (ρR), le centre étant beaucoup plus encombré que les régions externes. Les barres colorées indiquent le nombre d'atomes d'hydrogène (nH) dans chaque zone, précisant où se situe la majeure partie du matériel protéique. L'ensemble démontre que les protéines sont plus étroitement compactées au centre, ce qui limite leur mobilité, tandis que celles situées près des bords disposent de plus d'espace et se déplacent plus librement. Crédit : Proc. Natl. Acad. Sci. U.S.A. (2026).
Les simulations numériques permettent d'expliquer l'origine de ce comportement en reliant le mouvement observé à la structure interne des assemblages. Elles démontrent que ces derniers ne sont pas uniformes : le centre forme une zone dense et étroitement compactée, tandis que les couches externes sont moins encombrées. Cette variation structurelle entraîne directement des différences de mobilité, le mouvement étant plus lent dans le cœur dense et plus libre près de la périphérie. Il est important de noter que cette transition est graduelle : la mobilité évolue de manière continue du centre vers l'extérieur, et ne bascule pas brusquement entre deux comportements distincts.
Ce phénomène, appelé diffusion non fickienne, montre que l'organisation interne de l'assemblage façonne directement la dynamique des protéines. Comme le mouvement varie à travers la structure, il ne peut être décrit par une loi de diffusion unique, illustrant ainsi les limites des modèles simplifiés pour décrire le mouvement moléculaire dans des environnements biologiques encombrés.
De la structure au mouvement
Ces résultats démontrent comment l'organisation des protéines à l'échelle nanométrique peut influencer directement leur mobilité et leurs interactions. De tels effets sont susceptibles de jouer un rôle crucial au sein des cellules vivantes, où les molécules opèrent rarement de manière isolée, mais évoluent dans des environnements encombrés et structurés.
Au-delà de ce système spécifique, ces travaux soulignent les limites des modèles de diffusion simplifiés pour décrire le mouvement moléculaire dans des milieux complexes. Lorsque la structure locale varie, comme c'est le cas dans de nombreux systèmes biologiques ou de la matière molle, le mouvement ne peut plus être résumé par une description unique et uniforme.
En révélant ces effets par l'expérience, la diffusion de neutrons offre un moyen puissant de lier l'organisation moléculaire à la dynamique. Elle contribue ainsi à construire une vision plus réaliste du fonctionnement des systèmes biologiques à l'échelle microscopique.
Reference :
L.M. Miñarro, S. Chakraborty, C. Beck, A.C. Grundel, I. Mosca, F. Roosen-Runge, T.I. Morozova, J. Barrat, F. Schreiber, & T. Seydel, Non-Fickian diffusion within assemblies of the intrinsically disordered protein β-casein, Proc. Natl. Acad. Sci. U.S.A. 123 (11) e2532636123, (2026). DOI: 10.1073/pnas.2532636123
Instrument ILL : IN16B
Contact ILL : Tilo Seydel
Institutions impliquées : Université Grenoble-Alpes, University of Tübingen, Heidelberg University, Lund University and École Normale Supérieure de Lyon